

冠状动脉粥样硬化性心脏病(冠心病)是全球范围内导致死亡和残疾的首要心血管疾病。如何早期精准识别高风险人群是心血管疾病防治的核心难题。临床上常用的风险标志物低密度脂蛋白胆固醇(LDL-C)并不能全面反映LDL颗粒的致动脉粥样硬化效应。因此,临床上急需可直接反映动脉粥样硬化内在生物学过程的新型标志物。
中国科学院昆明动物研究所赖仞研究员团队长期聚焦先天免疫分子Cathelicidin抗菌肽LL-37在心血管疾病中的功能研究。前期工作中,该团队发现LL-37可通过与线粒体DNA形成复合物,驱动动脉粥样硬化中的炎症激活(Immunity, 2015),并证实LL-37能直接结合LDL的核心载脂蛋白ApoB-100,通过肝脏途径促进LDL清除(Science China Life Sciences, 2025)。在最新研究中,赖仞研究员团队联合加拿大多伦多大学倪合宇教授团队、昆明医科大学第一附属医院段勇教授团队研究发现,循环中的LL-37-ApoB-100复合物水平可作为冠心病独立且强效的预测因子。
研究团队首先明确了LL-37与ApoB-100之间存在多位点、高亲和力的直接结合。在此基础上,制备了可特异性识别该复合物的多克隆抗体,并证实该复合物在动脉粥样硬化斑块及患者血浆中显著富集。基于冠状动脉造影受试者的病例-对照研究,研究团队发现血浆LL-37–ApoB-100复合物水平在冠心病患者中显著升高。经两个独立中心交叉验证,该复合物水平与血管狭窄严重度评分呈强正相关。随着复合物水平的升高,冠心病风险呈明显的等级递增趋势,展现出独立于传统危险因素的预测价值。该发现弥补了现有血脂检测的短板,为精准地评估心血管风险提供了新工具。
该成果于2026年4月以“LL-37-ApoB-100 Complex Serves as a Biomarker of Coronary Artery Disease”为题,在线发表于国际知名学术期刊 Arteriosclerosis, Thrombosis, and Vascular Biology(ATVB)。中国科学院昆明动物研究所赖仞研究员与加拿大多伦多大学倪合宇教授为本文的共同通讯作者;中国科学院昆明动物研究所房亚群副研究员、张治业副研究员(现为中国医学科学院医学生物学研究所研究员)、硕士研究生曹奇奇,以及昆明医科大学第一附属医院李娅教授(现为云南大学附属医院检验科主任)、段勇教授为本文的共同第一作者。此外,昆明医科大学附属延安医院的孟平副研究员、李亚雄教授和昆明动物研究所李明研究员、马占山研究员也参与了该研究。该研究得到了国家重点研发计划、国家自然科学基金委员会、中国科学院、云南省科技厅、昆明市科技局以及新基石研究员等项目的资助。
加州大学圣地亚哥分校Sotirios Tsimikas教授在同刊发表的专家述评中指出:该研究将脂蛋白生物学与固有免疫整合起来,为理解动脉粥样硬化的发生发展及风险评估提供了全新视角(DOI: 10.1161/ATVBAHA.126.324779)。
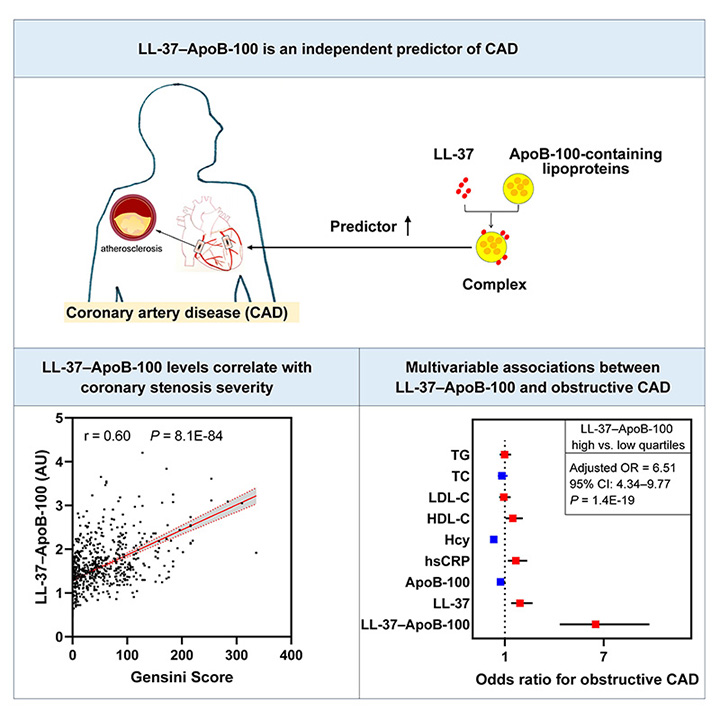
循环中的LL-37-ApoB-100复合物水平可作为冠心病独立且强效的预测因子
文章链接:https://www.ahajournals.org/doi/10.1161/ATVBAHA.125.323486?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
